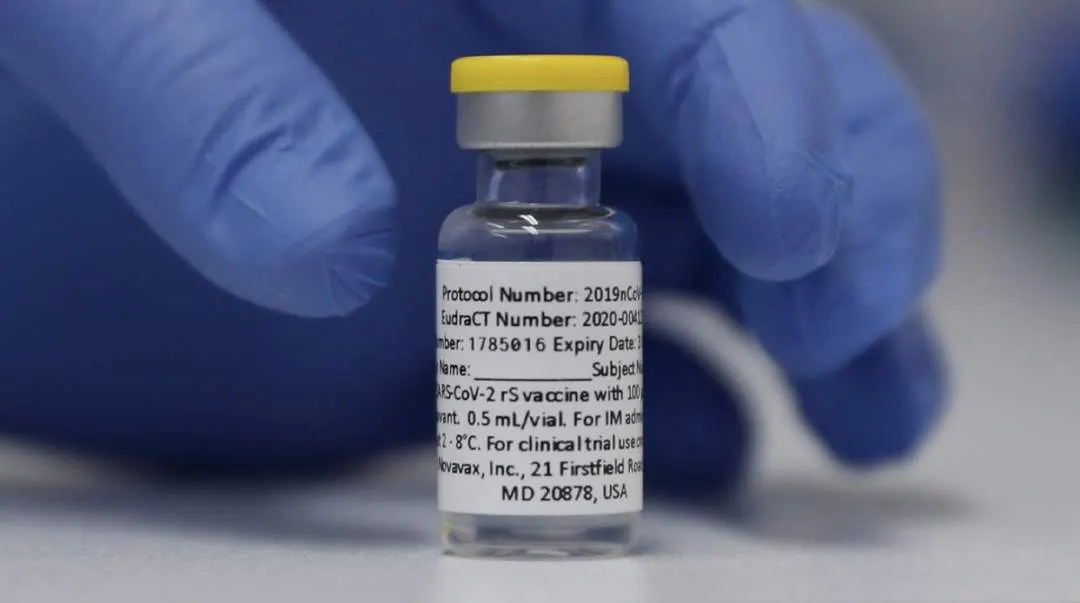
Novavax ขออนุมัติฉุกเฉิน สำหรับวัคซีน COVID-19 ในประเทศยากจนก่อน

วัคซีน Novavax ได้ขอให้หน่วยงานกำกับดูแลในประเทศอินเดีย อินโดนีเซียและฟิลิปปินส์ ที่จะอนุญาตให้ใช้ในกรณีฉุกเฉินของวัคซีน COVID-19 นำเสนอการฉีดไปยังบางประเทศที่มีรายได้ต่ำก่อนประเทศที่เต็มไปด้วยอุปกรณ์ที่เพียงพอ
Novavax ซึ่งมีฐานอยู่ในสหรัฐฯ ร่วมมือกับ Serum Institute of India เพื่อสมัครใน 3 ประเทศ และวางแผนในปลายเดือนนี้ เพื่อขอการทบทวนจากองค์การอนามัยโลก (WHO) เพื่อเป็นส่วนหนึ่งของโครงการวัคซีนทั่วโลกของ COVAX
สแตนลีย์ เอิร์ค ซีอีโอของ Novavax เรียกสิ่งที่ส่งมาด้วย “ขั้นตอนสำคัญในการเข้าถึงวัคซีนที่ปลอดภัยและมีประสิทธิภาพหลายล้านโดส สำหรับประเทศที่มีความจำเป็นเร่งด่วนในการควบคุมโรคระบาด”
บริษัทประกาศว่า มีแผนจะส่งใบสมัครในสหราชอาณาจักรเร็วๆ นี้ ตามด้วยยุโรป ออสเตรเลีย แคนาดา และนิวซีแลนด์ แต่ไม่ใช่ในสหรัฐอเมริกาจนกว่าจะถึงปลายปี
Novavax two-dose shot ทำจากสำเนาโปรตีนสไปค์ที่ปลูกในห้องปฏิบัติการซึ่งเคลือบ coronavirus
ซึ่งแตกต่างจากวัคซีนที่ใช้กันอย่างแพร่หลายอื่น ๆ มาก ซึ่งส่งคำสั่งทางพันธุกรรมสำหรับร่างกายเพื่อสร้างโปรตีนสไปค์ของตัวเอง
วัคซีน Novavax จัดเก็บและขนส่งได้ง่ายกว่าตัวเลือกอื่นๆ และคาดว่าจะมีบทบาทสำคัญในการเพิ่มอุปทานในประเทศยากจนที่ต้องการวัคซีนมากขึ้น
ในเดือนมิถุนายน Novavax ประกาศว่า วัคซีนได้พิสูจน์แล้วประมาณ 90% ว่ามีประสิทธิภาพในการต้าน COVID-19 ตามอาการ ในการศึกษาผู้ป่วยเกือบ 30,000 คนในสหรัฐอเมริกาและเม็กซิโก
มันยังทำงานกับสายพันธุ์ที่หมุนเวียนในประเทศเหล่านั้นในขณะนั้น ผลข้างเคียงส่วนใหญ่ไม่รุนแรง
สำหรับสายพันธุ์เดลต้าที่แพร่ระบาดได้สูง ซึ่งขณะนี้กำลังแพร่ระบาดไปทั่วโลก Novavax ยังประกาศในชั่วข้ามคืนว่า การให้บูสเตอร์ 6 เดือน หลังจากการฉีดครั้งที่ 2 ช่วยเพิ่มแอนติบอดีในการต่อสู้กับไวรัสที่สามารถจัดการกับการกลายพันธุ์นั้นได้
การศึกษาเพิ่มเติมในสหราชอาณาจักรและที่อื่น ๆ กำลังทดสอบว่า วัคซีน Novavax สามารถใช้เป็นตัวกระตุ้นหลังจากวัคซีน COVID-19 ชนิดอื่นได้หรือไม่
นายเอิร์กกล่าวว่า ข้อมูลแบบผสมและจับคู่อาจทำให้วัคซีนกลายเป็น "ตัวกระตุ้นทางเลือกสากล" ในประเทศร่ำรวย และบริษัทกล่าวว่า อินโดนีเซียได้แสดงความสนใจที่จะใช้วัคซีน Novavax เป็นตัวกระตุ้นหลังจากฉีดวัคซีนที่ผลิตในจีน
บริษัท Gaithersburg รัฐแมริแลนด์ กล่าวว่า บริษัทกำลังดำเนินการผลิต 100 ล้านโดสต่อเดือนภายในสิ้นไตรมาสที่ 3 และ 150 ล้านโดสต่อเดือนภายในสิ้นปี
 สำนักงานพุทธฯ สั่งตรวจสอบ พ่อแม่ "น้องไนซ์" เชื่อมจิต
สำนักงานพุทธฯ สั่งตรวจสอบ พ่อแม่ "น้องไนซ์" เชื่อมจิต เขมรเตรียมฉาย หนังบางระจันเวอร์ชั่นเขมร อ้างหมู่บ้านบางระจันมีที่มาจากกัมพูชา!
เขมรเตรียมฉาย หนังบางระจันเวอร์ชั่นเขมร อ้างหมู่บ้านบางระจันมีที่มาจากกัมพูชา! หนุ่มเครียด! แฟนไปทำศัลยกรรม แล้วหน้าตลกจนไม่มีอารมณ์..ด้วย?
หนุ่มเครียด! แฟนไปทำศัลยกรรม แล้วหน้าตลกจนไม่มีอารมณ์..ด้วย? เอาอีกแล้ว! เขมรก็อปปี้หนังไทย เรื่องเด็กหญิงวัลลี ยอดกตัญญู?
เอาอีกแล้ว! เขมรก็อปปี้หนังไทย เรื่องเด็กหญิงวัลลี ยอดกตัญญู? วิธีกินคอลลาเจนให้ได้ผลดีที่สุด
วิธีกินคอลลาเจนให้ได้ผลดีที่สุด หนุ่มกล้ามโตจีบสาว สาวไม่เล่นด้วย เลยจับสาวทุ่มลงพื้น
หนุ่มกล้ามโตจีบสาว สาวไม่เล่นด้วย เลยจับสาวทุ่มลงพื้น detain: กักขัง ควบคุมตัว
detain: กักขัง ควบคุมตัว เมื่อสาวเจอความทรงจำที่หายไป..มาอยู่ที่ใต้สะพานลอย
เมื่อสาวเจอความทรงจำที่หายไป..มาอยู่ที่ใต้สะพานลอย นักเรียนมุสลิมในเยอรมันเผย "ศาสนาของเรา อยู่เหนือกฎหมาย!!"
นักเรียนมุสลิมในเยอรมันเผย "ศาสนาของเรา อยู่เหนือกฎหมาย!!" เอาอีกแล้ว! เขมรก็อปปี้หนังไทย เรื่องเด็กหญิงวัลลี ยอดกตัญญู?
เอาอีกแล้ว! เขมรก็อปปี้หนังไทย เรื่องเด็กหญิงวัลลี ยอดกตัญญู? เมื่อหนูน้อยทำตุ๊กตา "ลาบูบู้"..เพราะรู้ซื้อไม่ได้ มันราคาแพง!
เมื่อหนูน้อยทำตุ๊กตา "ลาบูบู้"..เพราะรู้ซื้อไม่ได้ มันราคาแพง! ”ดอนเมือง“ ถูกยก สนามบินดีที่สุดในโลกอันดับ 10 ของสายการบินต้นทุนต่ำ
”ดอนเมือง“ ถูกยก สนามบินดีที่สุดในโลกอันดับ 10 ของสายการบินต้นทุนต่ำ อีก 50 ปีข้างหน้า ไทยจะ "ร้อนเท่าทะเลทรายซาฮาร่า"
อีก 50 ปีข้างหน้า ไทยจะ "ร้อนเท่าทะเลทรายซาฮาร่า"